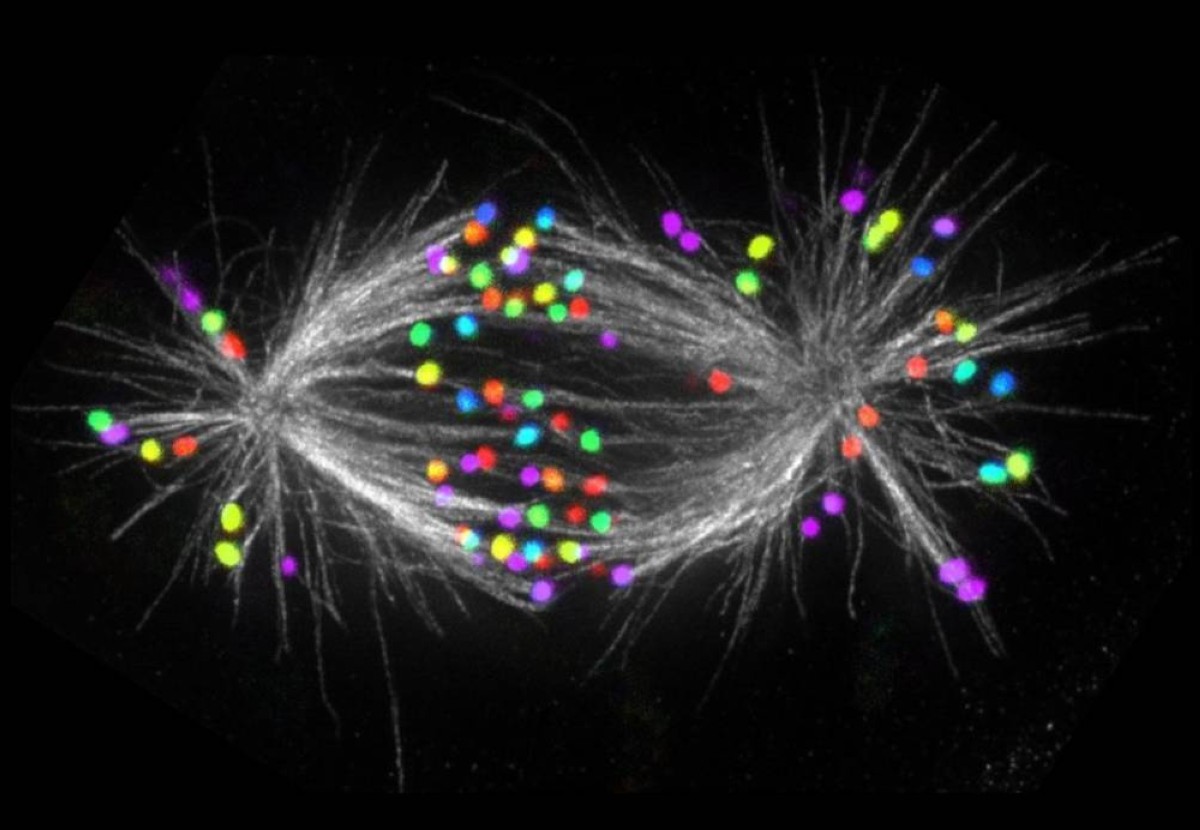
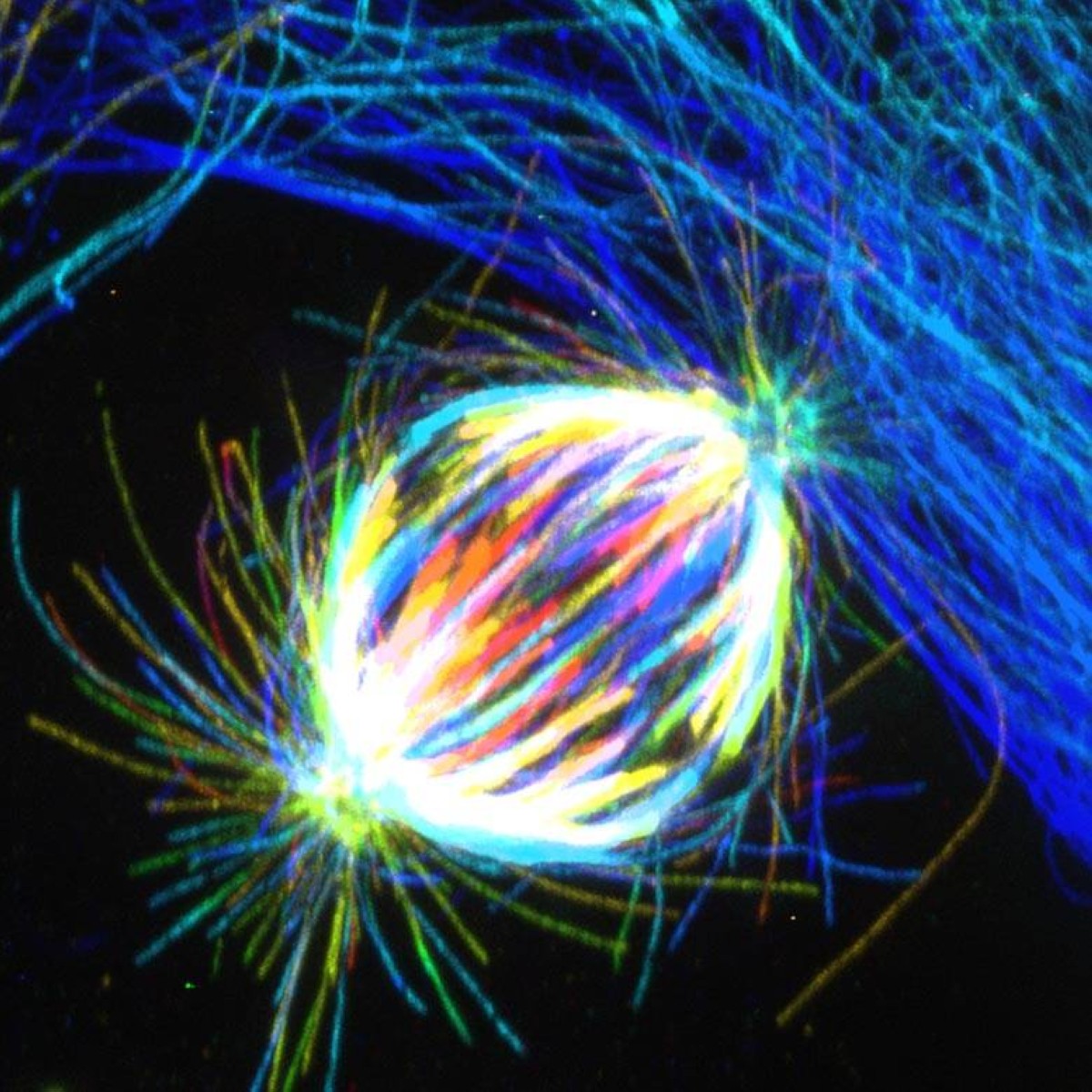
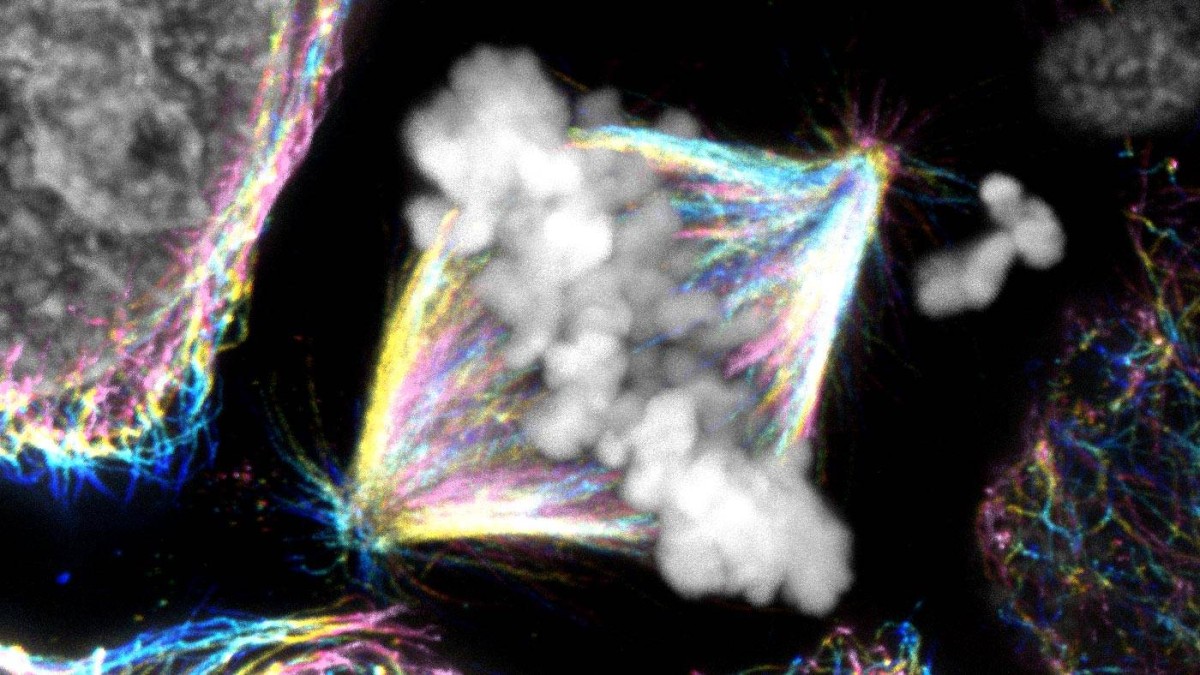
في اختراق علمي غير مسبوق، أعلن فريق بحثي من معهد رودر بوشكوفيتش (RBI) في زغرب – كرواتيا عن اكتشاف ينسف أكثر من عشرين عاما من المعلومات المستقرة في الكتب الدراسية حول آلية انقسام الخلية، أحد أهم العمليات الحيوية في جسم الإنسان.
وكشفت الدراستان، المنشورتان في دورية Nature Communications، عن وظيفة جديدة لبروتين CENP-E تُعدّ إعادة صياغة جذرية للفهم التقليدي لهذه العملية المعقدة.
لطالما اعتُبر بروتين CENP-E بمثابة "المحرّك" الذي يسحب الكروموسومات المتأخرة إلى منتصف الخلية قبل انقسامها.
هذا التفسير البسيط ظل ثابتا لعقود، لكن فريق الباحثَين الدكتور كرونو فوكوشتش والأستاذة إيفا توليتش كشف أن هذا الدور كان في الحقيقة قراءة ناقصة.
ويظهر من خلال التجارب الحديثة أن البروتين لا يعمل كمحرك، بل كمنظّم أساسي يضمن تثبيت الارتباط الأولي بين الكروموسومات وألياف الهيكل الداخلي للخلية، وهي خطوة حاسمة لضمان اصطفاف الكروموسومات بدقة قبل فصلها، وبدون هذا التثبيت، تتعطل العملية منذ بدايتها، مما يرفع احتمالات وقوع أخطاء قد تقود إلى أمراض خطيرة، وفقا لـ scitechdaily.
وتبرز أهمية هذا الاكتشاف عندما يُنظر إلى دور Aurora kinases، وهي مجموعة بروتينات تعمل كإشارات مرور حيوية داخل الخلية، فهذه البروتينات تُكثر من إرسال "إشارات حمراء" تمنع الارتباطات الخاطئة خلال المرحلة المبكرة من الانقسام، لكنها قد تتسبب أيضا في تعطيل الارتباطات الصحيحة، هنا يتدخل CENP-E ليعمل كعامل موازن، مخفّضا من تأثير الإشارات الحمراء ومتيحا الفرصة لتكوين الارتباط المستقر الأول، وهو الشرط الضروري لانطلاق عملية الانقسام بسلاسة.
ويؤكد الباحثون أن النتائج الجديدة لا تعدّل مجرد تفاصيل تقنية، بل تغيّر الإطار النظري الكامل لآلية اصطفاف الكروموسومات داخل الخلية، فبدل التركيز على القوة الميكانيكية وسحب الكروموسومات، ينتقل الفهم العلمي الآن إلى نموذج يتناول التنظيم الدقيق والتوقيت الحسّاس للارتباطات الأولية.
وتكمن خطورة أي خلل في هذه العملية في كونها مرتبطة مباشرة بالسرطان والاضطرابات الجينية، فالخلايا السرطانية غالبا ما تحمل كروموسومات مكررة أو مفقودة، وهي علامات واضحة على فشل في نظام "المرور الخلوي".
ومن خلال الربط بين نشاط Aurora kinases ودور CENP-E، يفتح هذا الاكتشاف الباب أمام تطوير علاجات جديدة تستهدف هذه الآليات الحيوية أو تضبطها بدقة.
وقد تم دعم هذا العمل البحثي من خلال منحة Synergy المرموقة من المجلس الأوروبي للبحث، إضافة إلى مؤسسة العلوم الكرواتية ومشاريع أوروبية مشتركة.
ويؤكد الفريق أن التقدّم لم يكن ممكنا دون استخدام بنية حوسبة متطورة وجهاز تصوير بيولوجي عالي الدقة.
ويقول فوكوشتش: "نحن لا نعيد كتابة نموذج علمي فحسب، بل نكشف آلية ترتبط مباشرة بالمرض وتفتح فرصا علاجية جديدة"، فيما تضيف توليتش: "فهم كيفية تعاون هذه المنظّمات الميكروسكوبية يمثل خطوة أساسية نحو علاج الإخفاقات التي تؤدي إلى السرطان".
بهذا الإنجاز، يضع العلماء من زغرب حجر أساس جديدا لفهم أكثر دقة لآلية انقسام الخلية، ويمهّدون الطريق لمقاربات علاجية مستقبلية قد تغيّر مسار الطب الحديث.